நோபல் வாயு, கால அட்டவணையின் குழு 18 (VIIIa) ஐ உருவாக்கும் ஏழு வேதியியல் கூறுகளில் ஏதேனும் ஒன்று. ஹீலியம் (He), நியான் (Ne), ஆர்கான் (Ar), கிரிப்டன் (Kr), செனான் (Xe), ரேடான் (Rn) மற்றும் oganesson (Og) ஆகிய கூறுகள் அவை. உன்னத வாயுக்கள் நிறமற்றவை, மணமற்றவை, சுவையற்றவை, எரியாத வாயுக்கள். அவை பாரம்பரியமாக குறிப்பிட்ட கால இடைவெளியில் குழு 0 என்று பெயரிடப்பட்டுள்ளன, ஏனெனில் அவை கண்டுபிடிக்கப்பட்ட பல தசாப்தங்களாக அவை மற்ற அணுக்களுடன் பிணைக்க முடியாது என்று நம்பப்பட்டது; அதாவது, அவற்றின் அணுக்கள் மற்ற உறுப்புகளுடன் ஒன்றிணைந்து வேதியியல் சேர்மங்களை உருவாக்க முடியவில்லை. அவற்றின் மின்னணு கட்டமைப்புகள் மற்றும் அவற்றில் சில உண்மையில் சேர்மங்களை உருவாக்குகின்றன என்பதைக் கண்டுபிடிப்பது மிகவும் பொருத்தமான பதவிக்கு வழிவகுத்தது, குழு 18.
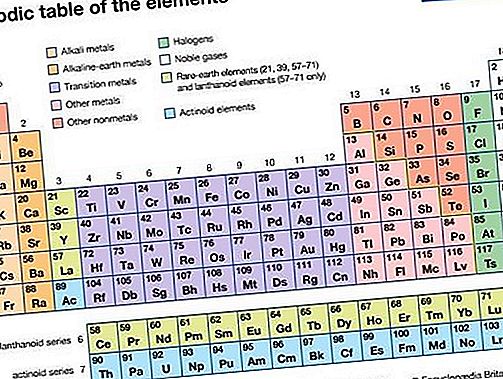
குழுவின் உறுப்பினர்கள் கண்டுபிடிக்கப்பட்டு அடையாளம் காணப்பட்டபோது, அவை மிகவும் அரிதானவை, அதே போல் வேதியியல் மந்தமானவை என்று கருதப்பட்டது, எனவே அவை அரிதான அல்லது மந்த வாயுக்கள் என்று அழைக்கப்பட்டன. எவ்வாறாயினும், இந்த உறுப்புகள் பல பூமியிலும், பிரபஞ்சத்தின் பிற பகுதிகளிலும் ஏராளமாக உள்ளன என்பது இப்போது அறியப்படுகிறது, எனவே அரிதான பதவி தவறாக வழிநடத்துகிறது. இதேபோல், மந்தம் என்ற வார்த்தையின் பயன்பாடு குறைபாட்டைக் கொண்டுள்ளது, இது வேதியியல் செயலற்ற தன்மையைக் குறிக்கிறது, இது குழு 18 இன் சேர்மங்களை உருவாக்க முடியாது என்று கூறுகிறது. வேதியியல் மற்றும் ரசவாதத்தில், நோபல் என்ற சொல் நீண்ட காலமாக வேதியியல் எதிர்வினைக்கு உட்படுத்த தங்கம் மற்றும் பிளாட்டினம் போன்ற உலோகங்களின் தயக்கத்தைக் குறிக்கிறது; இங்கே மூடப்பட்டிருக்கும் வாயுக்களின் குழுவிற்கும் இது பொருந்தும்.
அவற்றின் அணு எண்கள் அதிகரிக்கும் போது உன்னத வாயுக்களின் மிகுதி குறைகிறது. ஹைட்ரஜன் தவிர பிரபஞ்சத்தில் ஹீலியம் மிகுதியாக உள்ளது. அனைத்து உன்னத வாயுக்களும் பூமியின் வளிமண்டலத்தில் உள்ளன, ஹீலியம் மற்றும் ரேடான் தவிர, அவற்றின் முக்கிய வணிக ஆதாரம் காற்று, அவற்றில் இருந்து அவை திரவமாக்கல் மற்றும் பகுதியளவு வடிகட்டுதல் மூலம் பெறப்படுகின்றன. பெரும்பாலான ஹீலியம் சில இயற்கை எரிவாயு கிணறுகளிலிருந்து வணிக ரீதியாக உற்பத்தி செய்யப்படுகிறது. ரேடியம் பொதுவாக ரேடியம் சேர்மங்களின் கதிரியக்க சிதைவின் விளைவாக தனிமைப்படுத்தப்படுகிறது. ரேடியம் அணுக்களின் கருக்கள் ஆற்றல் மற்றும் துகள்கள், ஹீலியம் கருக்கள் (ஆல்பா துகள்கள்) மற்றும் ரேடான் அணுக்களை வெளியேற்றுவதன் மூலம் தன்னிச்சையாக சிதைகின்றன. உன்னத வாயுக்களின் சில பண்புகள் அட்டவணையில் பட்டியலிடப்பட்டுள்ளன.
உன்னத வாயுக்களின் சில பண்புகள்
| கதிர்வளி | நியான் | ஆர்கான் | கிரிப்டன் | xenon | ரேடான் | ununoctium | |
|---|---|---|---|---|---|---|---|
| * 25.05 வளிமண்டலங்களில். | |||||||
| ** hcp = அறுகோண நெருக்கமான, fcc = முகத்தை மையமாகக் கொண்ட கன (கன நெருக்கமான-நிரம்பிய). | |||||||
| *** நிலையான ஐசோடோப்பு. | |||||||
| அணு எண் | 2 | 10 | 18 | 36 | 54 | 86 | 118 |
| அணு எடை | 4.003 | 20.18 | 39.948 | 83.8 | 131.293 | 222 | 294 *** |
| உருகும் இடம் (° C) | −272.2 * | −248.59 | −189.3 | −157.36 | −111.7 | −71 | - |
| கொதிநிலை (° C) | −268.93 | −246.08 | −185.8 | −153.22 | −108 | −61.7 | - |
| அடர்த்தி 0 ° C, 1 வளிமண்டலம் (லிட்டருக்கு கிராம்) | 0.17847 | 0.899 | 1.784 | 3.75 | 5.881 | 9.73 | - |
| 20 ° C வெப்பநிலையில் நீரில் கரைதிறன் (1,000 கிராம் தண்ணீருக்கு கன சென்டிமீட்டர் வாயு) | 8.61 | 10.5 | 33.6 | 59.4 | 108.1 | 230 | - |
| ஐசோடோபிக் மிகுதி (நிலப்பரப்பு, சதவீதம்) | 3 (0.000137), 4 (99.999863) | 20 (90.48), 21 (0.27), 22 (9.25) | 36 (0.3365), 40 (99.6003) | 78 (0.35), 80 (2.28), 82 (11.58), 83 (11.49), 84 (57), 86 (17.3) | 124 (0.09), 126 (0.09), 128 (1.92), 129 (26.44), 130 (4.08), 131 (21.18), 132 (26.89), 134 (10.44), 136 (8.87) | - | - |
| கதிரியக்க ஐசோடோப்புகள் (வெகுஜன எண்கள்) | 5-10 | 16–19, 23–34 | 30–35, 37, 39, 41–53 | 69–77, 79, 81, 85, 87–100 | 110–125, 127, 133, 135–147 | 195–228 | 294 |
| வாயு வெளியேற்றக் குழாயால் வெளிப்படும் ஒளியின் நிறம் | மஞ்சள் | சிவப்பு | சிவப்பு அல்லது நீலம் | மஞ்சள்-பச்சை | நீலம் முதல் பச்சை வரை | - | - |
| இணைவு வெப்பம் (ஒரு மோலுக்கு கிலோஜூல்கள்) | 0.02 | 0.34 | 1.18 | 1.64 | 2.3 | 3 | - |
| ஆவியாதல் வெப்பம் (ஒரு மோலுக்கு கலோரிகள்) | 0.083 | 1.75 | 6.5 | 9.02 | 12.64 | 17 | - |
| குறிப்பிட்ட வெப்பம் (ஒரு கிராம் கெல்வின் ஜூல்ஸ்) | 5.1931 | 1.03 | 0.52033 | 0.24805 | 0.15832 | 0.09365 | - |
| சிக்கலான வெப்பநிலை (கே) | 5.19 | 44.4 | 150.87 | 209.41 | 289.77 | 377 | - |
| சிக்கலான அழுத்தம் (வளிமண்டலங்கள்) | 2.24 | 27.2 | 48.34 | 54.3 | 57.65 | 62 | - |
| சிக்கலான அடர்த்தி (ஒரு கன சென்டிமீட்டருக்கு கிராம்) | 0.0696 | 0.4819 | 0.5356 | 0.9092 | 1.103 | - | - |
| வெப்ப கடத்துத்திறன் (மீட்டருக்கு வாட்ஸ் கெல்வின்) | 0.1513 | 0.0491 | 0.0177 | 0.0094 | 0.0057 | 0.0036 | - |
| காந்த பாதிப்பு (ஒரு மோலுக்கு cgs அலகுகள்) | −0.0000019 | −0.0000072 | −0.0000194 | −0.000028 | −0.000043 | - | - |
| படிக அமைப்பு ** | hcp | fcc | fcc | fcc | fcc | fcc | - |
| ஆரம்: அணு (ஆங்ஸ்ட்ரோம்ஸ்) | 0.31 | 0.38 | 0.71 | 0.88 | 1.08 | 1.2 | - |
| ஆரம்: கோவலன்ட் (படிக) மதிப்பிடப்பட்ட (ஆங்ஸ்ட்ரோம்ஸ்) | 0.32 | 0.69 | 0.97 | 1.1 | 1.3 | 1.45 | - |
| நிலையான துருவமுனைப்பு (கன ஆங்ஸ்ட்ரோம்கள்) | 0.204 | 0.392 | 1.63 | 2.465 | 4.01 | - | - |
| அயனியாக்கம் திறன் (முதல், எலக்ட்ரான் வோல்ட்) | 24.587 | 21.565 | 15.759 | 13.999 | 12.129 | 10.747 | - |
| எலக்ட்ரோநெக்டிவிட்டி (பாலிங்) | 4.5 | 4.0 | 2.9 | 2.6 | 2.25 | 2.0 | - |













![ஹாக்ஸின் பிக் ஸ்லீப் படம் [1946] ஹாக்ஸின் பிக் ஸ்லீப் படம் [1946]](https://images.thetopknowledge.com/img/entertainment-pop-culture/6/big-sleep-film-hawks-1946.jpg)