ஆக்ஸியாசிட், ஆக்ஸிஜன் கொண்ட எந்த அமிலமும். பெரும்பாலான கோவலன்ட் அல்லாத மெட்டல் ஆக்சைடுகள் தண்ணீருடன் வினைபுரிந்து அமில ஆக்சைடுகளை உருவாக்குகின்றன; அதாவது, அவை தண்ணீருடன் வினைபுரிந்து ஆக்ஸைசிட்களை உருவாக்குகின்றன, அவை ஹைட்ரோனியம் அயனிகளை (H 3 O +) கரைசலில் விளைவிக்கின்றன. கார்பன் மோனாக்சைடு, CO, நைட்ரஸ் ஆக்சைடு, N 2 O, மற்றும் நைட்ரிக் ஆக்சைடு, NO போன்ற சில விதிவிலக்குகள் உள்ளன.
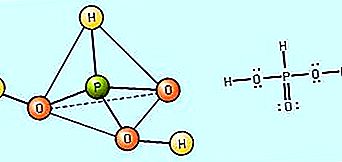
ஒரு ஆக்ஸியாசிட்டின் வலிமை அது தண்ணீரில் எந்த அளவிற்குப் பிரிகிறது என்பதன் மூலம் வரையறுக்கப்படுகிறது (அதாவது, H + அயனிகளை உருவாக்கும் திறன்). பொதுவாக, ஆக்ஸியாசிட்களின் ஒப்பீட்டு வலிமையை மையமற்ற அணுவின் எலக்ட்ரோநெக்டிவிட்டி மற்றும் ஆக்ஸிஜனேற்ற எண்ணின் அடிப்படையில் கணிக்க முடியும். மத்திய அணுவின் எலக்ட்ரோநெக்டிவிட்டி அதிகரிக்கும் போது அமில வலிமை அதிகரிக்கிறது. எடுத்துக்காட்டாக, குளோரின் (Cl) இன் எலக்ட்ரோநெக்டிவிட்டி சல்பர் (S) ஐ விட அதிகமாக இருப்பதால், இது பாஸ்பரஸ் (P) ஐ விட அதிகமாக இருப்பதால், பெர்க்ளோரிக் அமிலம், HClO 4, ஒரு வலுவான அமிலம் என்று கணிக்க முடியும் சல்பூரிக் அமிலம், H 2 SO 4, இது பாஸ்போரிக் அமிலத்தை விட வலுவான அமிலமாக இருக்க வேண்டும், H 3 PO 4. கொடுக்கப்பட்ட nonmetal மத்திய அணுவுக்கு, மத்திய அணுவின் ஆக்சிஜனேற்றம் எண்ணிக்கை அதிகரிக்கும்போது அமில வலிமை அதிகரிக்கிறது. எடுத்துக்காட்டாக, நைட்ரஜன் அமிலம், HNO 3, இதில் நைட்ரஜன் (N) அணு +5 ஆக்சிஜனேற்ற எண்ணைக் கொண்டுள்ளது, இது நைட்ரஸ் அமிலத்தை விட வலுவான அமிலமாகும், HNO 2, அங்கு நைட்ரஜன் ஆக்சிஜனேற்ற நிலை +3 ஆகும். அதே வழியில், சல்பூரிக் அமிலம், H 2 SO 4, அதன் +6 ஆக்சிஜனேற்ற நிலையில் கந்தகத்துடன், கந்தக அமிலமான H 2 SO 3 ஐ விட வலுவான அமிலமாகும், அங்கு +4 ஆக்சிஜனேற்றம் எண் கந்தகம் உள்ளது.
ஆக்ஸியாசிட்டின் உப்பு என்பது அமிலம் ஒரு தளத்துடன் வினைபுரியும் போது உருவாகும் ஒரு கலவை ஆகும்: அமிலம் + அடிப்படை → உப்பு + நீர். இந்த வகை எதிர்வினை நடுநிலைப்படுத்தல் என்று அழைக்கப்படுகிறது, ஏனெனில் தீர்வு நடுநிலையானது.













