ஃவுளூரின் (எஃப்), மிகவும் எதிர்வினை வேதியியல் உறுப்பு மற்றும் ஆலசன் உறுப்புகளின் லேசான உறுப்பினர் அல்லது கால அட்டவணையின் குழு 17 (குழு VIIa). எலக்ட்ரான்களை ஈர்க்கும் அதன் தீவிர திறனுக்கு ரசாயன செயல்பாடு காரணமாக இருக்கலாம் (இது மிகவும் எலக்ட்ரோநெக்டிவ் உறுப்பு) மற்றும் அதன் அணுக்களின் சிறிய அளவிற்கு.
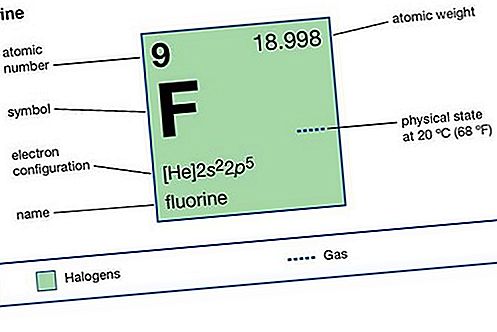
உறுப்பு பண்புகள்
| அணு எண் | 9 |
|---|---|
| அணு எடை | 18.9984 |
| உருகும் இடம் | −219.62 ° C (−363.32 ° F) |
| கொதிநிலை | −188 ° C (−306 ° F) |
| அடர்த்தி (1 atm, 0 ° C அல்லது 32 ° F) | 1.696 கிராம் / லிட்டர் (0.226 அவுன்ஸ் / கேலன்) |
| ஆக்சிஜனேற்றம் நிலைகள் | −1 |
| எலக்ட்ரான் கட்டமைப்பு. | 1s 2 2s 2 2p 5 |
வரலாறு
ஃவுளூரின் கொண்ட தாது ஃவுளூஸ்பார் (அல்லது ஃவுளூரைட்) 1529 இல் ஜெர்மன் மருத்துவரும் கனிமவியலாளருமான ஜார்ஜியஸ் அக்ரிகோலா விவரித்தார். கச்சா ஹைட்ரோஃப்ளூரிக் அமிலம் முதன்முதலில் 1720 ஆம் ஆண்டில் அறியப்படாத ஒரு ஆங்கில கண்ணாடித் தொழிலாளியால் தயாரிக்கப்பட்டது என்று தெரிகிறது. 1771 ஆம் ஆண்டில் ஸ்வீடிஷ் வேதியியலாளர் கார்ல் வில்ஹெல்ம் ஷீல் ஒரு கண்ணாடி பதிலடியில் செறிவூட்டப்பட்ட சல்பூரிக் அமிலத்துடன் புளூஸ்பாரை வெப்பப்படுத்துவதன் மூலம் தூய்மையற்ற நிலையில் ஹைட்ரோஃப்ளூரிக் அமிலத்தைப் பெற்றார், இது பெரிதும் சிதைந்தது. பொருள்; இதன் விளைவாக, உலோகத்தால் செய்யப்பட்ட பாத்திரங்கள் பொருளின் அடுத்தடுத்த சோதனைகளில் பயன்படுத்தப்பட்டன. ஏறக்குறைய அன்ஹைட்ரஸ் அமிலம் 1809 ஆம் ஆண்டில் தயாரிக்கப்பட்டது, இரண்டு ஆண்டுகளுக்குப் பிறகு பிரெஞ்சு இயற்பியலாளர் ஆண்ட்ரே-மேரி ஆம்பேர் இது குளோரின் ஒத்த ஒரு அறியப்படாத உறுப்புடன் ஹைட்ரஜனின் கலவை என்று பரிந்துரைத்தார், இதற்காக அவர் ஃப்ளோரின் என்ற பெயரை பரிந்துரைத்தார். புளூஸ்பார் பின்னர் கால்சியம் ஃவுளூரைடு என்று அங்கீகரிக்கப்பட்டது.
ஃவுளூரைன் தனிமைப்படுத்தப்படுவது நீண்ட காலமாக கனிம வேதியியலில் தீர்க்கப்படாத பிரச்சினைகளில் ஒன்றாகும், மேலும் 1886 ஆம் ஆண்டு வரை பிரெஞ்சு வேதியியலாளர் ஹென்றி மொய்சன் ஹைட்ரஜன் ஃவுளூரைடில் பொட்டாசியம் ஹைட்ரஜன் ஃவுளூரைடு கரைசலை மின்னாற்பகுப்பு செய்வதன் மூலம் உறுப்பை தயாரித்தார். ஃவுளூரைனை தனிமைப்படுத்தியதற்காக 1906 ஆம் ஆண்டு வேதியியலுக்கான நோபல் பரிசைப் பெற்றார். உறுப்பு மற்றும் அதன் நச்சு பண்புகளை கையாளுவதில் உள்ள சிரமம் ஃவுளூரின் வேதியியலில் மெதுவான முன்னேற்றத்திற்கு பங்களித்தது. உண்மையில், இரண்டாம் உலகப் போரின் காலம் வரை இந்த உறுப்பு ஒரு ஆய்வக ஆர்வமாகத் தோன்றியது. எவ்வாறாயினும், யுரேனியம் ஐசோடோப்புகளைப் பிரிப்பதில் யுரேனியம் ஹெக்ஸாஃப்ளூரைட்டின் பயன்பாடு, தொழில்துறை முக்கியத்துவம் வாய்ந்த கரிம ஃவுளூரின் சேர்மங்களின் வளர்ச்சியுடன், ஃவுளூரைனை கணிசமான பயன்பாட்டின் தொழில்துறை இரசாயனமாக்கியது.
நிகழ்வு மற்றும் விநியோகம்
ஃவுளூரின் கொண்ட தாது ஃவுளூஸ்பார் (ஃவுளூரைட், சி.எஃப் 2) பல உலோகவியல் செயல்முறைகளில் ஒரு ஃப்ளக்ஸ் (சுத்திகரிப்பு முகவர்) ஆக பல நூற்றாண்டுகளாக பயன்படுத்தப்படுகிறது. ஃவுளூஸ்பார் என்ற பெயர் லத்தீன் ஃப்ளூயரிலிருந்து உருவானது, “பாய்கிறது.” தாது பின்னர் உறுப்புக்கான ஆதாரமாக நிரூபிக்கப்பட்டது, அதற்கேற்ப ஃவுளூரின் என்று பெயரிடப்பட்டது. ஃவுளூஸ்பாரின் நிறமற்ற, வெளிப்படையான படிகங்கள் ஒளிரும் போது ஒரு நீல நிறத்தை வெளிப்படுத்துகின்றன, மேலும் இந்த சொத்து அதற்கேற்ப ஃப்ளோரசன் என அழைக்கப்படுகிறது.
ஃப்ளோரின் இயற்கையில் அதன் வேதியியல் சேர்மங்களின் வடிவத்தில் மட்டுமே காணப்படுகிறது, ரேடியத்திலிருந்து கதிர்வீச்சுக்கு உட்படுத்தப்பட்ட ஃப்ளூஸ்பாரில் உள்ள இலவச தனிமத்தின் சுவடு அளவுகளைத் தவிர. ஒரு அரிய உறுப்பு அல்ல, இது பூமியின் மேலோட்டத்தில் 0.065 சதவிகிதம் ஆகும். ஃவுளூரின் கொண்டிருக்கும் தாதுக்கள் (1) ஃவுளூஸ்பார், இல்லினாய்ஸ், கென்டக்கி, டெர்பிஷைர், தெற்கு ஜெர்மனி, பிரான்சின் தெற்கே, மற்றும் ரஷ்யா மற்றும் ஃவுளூரின் முக்கிய மூலமான (2) கிரையோலைட் (நா 3 ஆல்எஃப் 6), முக்கியமாக கிரீன்லாந்திலிருந்து, (3) ஃப்ளோரோபாடைட் (Ca 5 [PO 4] 3 [F, Cl]), பரவலாக விநியோகிக்கப்பட்டு, ஃவுளூரின் மற்றும் குளோரின் மாறுபட்ட அளவுகளைக் கொண்டுள்ளது, (4) புஷ்பராகம் (அல் 2 சியோ 4 [F, OH] 2), ரத்தினக் கல், மற்றும் (5) லெபிடோலைட், ஒரு மைக்கா மற்றும் விலங்கு எலும்புகள் மற்றும் பற்களின் ஒரு கூறு.













