மீள் பண்புகள்
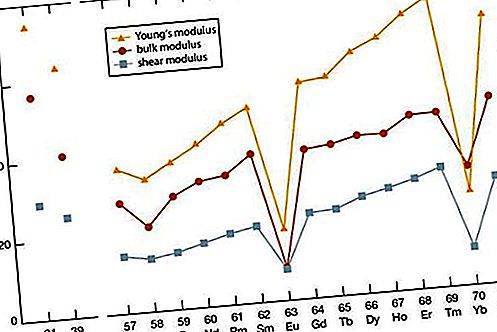
அரிய-பூமி உலோகங்களின் பிற பண்புகளைப் போலவே, அரிய-பூமி உலோகங்களின் மீள் மட்டு மற்ற உலோகக் கூறுகளின் நடுத்தர சதவிகிதத்தில் விழுகிறது. ஸ்காண்டியம் மற்றும் யட்ரியத்திற்கான மதிப்புகள் லாந்தனைடுகளின் (எர்பியம் முதல் லுடீடியம்) இறுதி உறுப்பினர்களின் மதிப்புகளைப் போலவே இருக்கும். அதிகரிக்கும் அணு எண்ணிக்கையுடன் மீள் மாடுலஸில் பொதுவான அதிகரிப்பு உள்ளது. சீரியம் (சில 4f பிணைப்பு), மற்றும் யெட்டர்பியம் (டிவலென்சி) ஆகியவற்றிற்கான முரண்பாடுகள் மதிப்புகள் தெளிவாக உள்ளன.
இயந்திர பண்புகளை
அரிதான-பூமி உலோகங்கள் பலவீனமானவை அல்ல, குறிப்பாக வலுவான உலோகக் கூறுகள் அல்ல, மேலும் அவை சில மிதமான தன்மையைக் காட்டுகின்றன. இயந்திர பண்புகள் உலோகங்களின் தூய்மை மற்றும் அவற்றின் வெப்ப வரலாற்றைப் பொறுத்து மிகவும் வலுவாக இருப்பதால், இலக்கியத்தில் அறிவிக்கப்பட்ட மதிப்புகளை ஒப்பிடுவது கடினம். இறுதி வலிமை சுமார் 120 முதல் 160 எம்.பி.ஏ (மெகாபாஸ்கல்கள்) மற்றும் டக்டிலிட்டி 15 முதல் 35 சதவீதம் வரை மாறுபடும். Ytterbium இன் வலிமை (யூரோபியம் அளவிடப்படவில்லை) 58 MPa, மற்றும் டக்டிலிட்டி உலோகத்திற்கு எதிர்பார்க்கப்படுவது போல 45 சதவிகிதம் அதிகமாக உள்ளது.
வேதியியல் பண்புகள்
அரிய-பூமி உலோகங்களின் காற்றின் வினைத்திறன் ஒளி லந்தனைடுகளுக்கும் கனமானவற்றுக்கும் இடையே குறிப்பிடத்தக்க வித்தியாசத்தை வெளிப்படுத்துகிறது. கனமான லந்தனைடுகள் (லுடீடியம் வழியாக காடோலினியம்), ஸ்காண்டியம் மற்றும் யட்ரியம் ஆகியவற்றைக் காட்டிலும் ஒளி லாந்தனைடுகள் மிக விரைவாக ஆக்ஸிஜனேற்றப்படுகின்றன. உருவான ஆக்சைடு உற்பத்தியின் மாறுபாடு காரணமாக இந்த வேறுபாடு ஒரு பகுதியாகும். ஒளி லந்தனைடுகள் (நியோடைமியம் வழியாக லந்தனம்) அறுகோண A- வகை R 2 O 3 கட்டமைப்பை உருவாக்குகின்றன; நடுத்தர லாந்தனைடுகள் (கடோலினியம் வழியாக சமாரியம்) மோனோக்ளினிக் பி-வகை ஆர் 2 ஓ 3 கட்டத்தை உருவாக்குகின்றன; கனமான லாந்தனைடுகள், ஸ்காண்டியம் மற்றும் யட்ரியம் ஆகியவை கன சி-வகை R 2 O 3 மாற்றத்தை உருவாக்குகின்றன. ஏ-வகை காற்றில் உள்ள நீராவியுடன் வினைபுரிந்து ஆக்ஸிஹைட்ராக்சைடை உருவாக்குகிறது, இது வெள்ளை பூச்சு சிதற காரணமாகிறது மற்றும் புதிய உலோக மேற்பரப்பை வெளிப்படுத்துவதன் மூலம் ஆக்சிஜனேற்றம் தொடர அனுமதிக்கிறது. சி-வகை ஆக்சைடு அலுமினியத்தின் நடத்தைக்கு ஒத்த, மேலும் ஆக்ஸிஜனேற்றத்தைத் தடுக்கும் இறுக்கமான, ஒத்திசைவான பூச்சு ஒன்றை உருவாக்குகிறது. பி-வகை ஆர் 2 ஓ 3 கட்டத்தை உருவாக்கும் சமாரியம் மற்றும் காடோலினியம், கனமான லாந்தனைடுகள், ஸ்காண்டியம் மற்றும் யட்ரியத்தை விட சற்று வேகமாக ஆக்ஸிஜனேற்றம் செய்கின்றன, ஆனால் இன்னும் ஒரு ஒத்திசைவான பூச்சு உருவாகின்றன, இது மேலும் ஆக்ஸிஜனேற்றத்தை நிறுத்துகிறது. இதன் காரணமாக, ஒளி லாந்தனைடுகள் வெற்றிடத்திலோ அல்லது மந்த வாயு வளிமண்டலத்திலோ சேமிக்கப்பட வேண்டும், அதே நேரத்தில் கனமான லாந்தனைடுகள், ஸ்காண்டியம் மற்றும் யட்ரியம் ஆகியவை எந்தவொரு ஆக்சிஜனேற்றமும் இல்லாமல் பல ஆண்டுகளாக திறந்தவெளியில் விடப்படலாம்.
பி.சி.சி அமைப்பைக் கொண்ட யூரோபியம் உலோகம், ஈரமான காற்றைக் கொண்ட எந்தவொரு அரிய பூமியிலும் மிக விரைவாக ஆக்ஸிஜனேற்றம் செய்கிறது மற்றும் ஒரு மந்த வாயு வளிமண்டலத்தில் எல்லா நேரங்களிலும் கையாளப்பட வேண்டும். ஈரப்பதமான காற்றில் வெளிப்படும் போது யூரோபியத்தின் எதிர்வினை தயாரிப்பு ஒரு ஹைட்ரேட் ஹைட்ராக்சைடு, யூ (ஓஎச்) 2 ― எச் 2 ஓ, இது ஒரு அசாதாரண எதிர்வினை தயாரிப்பு ஆகும், ஏனென்றால் மற்ற அரிய-பூமி உலோகங்கள் அனைத்தும் ஆக்சைடை உருவாக்குகின்றன.
உலோகங்கள் ஹைட்ரோஃப்ளூரிக் அமிலம் (எச்.எஃப்) தவிர அனைத்து அமிலங்களுடனும் தீவிரமாக வினைபுரிந்து, எச் 2 வாயுவை வெளியிட்டு அதனுடன் தொடர்புடைய அரிய-பூமி-அனானியன் கலவையை உருவாக்குகின்றன. ஹைட்ரோஃப்ளூரிக் அமிலத்தில் வைக்கப்படும் அரிய-பூமி உலோகங்கள் கரையாத RF 3 பூச்சு ஒன்றை உருவாக்குகின்றன, இது மேலும் எதிர்வினைகளைத் தடுக்கிறது.
அரிய-பூமி உலோகங்கள் உடனடியாக ஹைட்ரஜன் வாயுவுடன் வினைபுரிந்து RH 2 ஐ உருவாக்குகின்றன, மேலும் வலுவான ஹைட்ரைடிங் நிலைமைகளின் கீழ், RH 3 கட்டம் - ஸ்காண்டியம் தவிர, இது ஒரு ட்ரைஹைட்ரைடை உருவாக்குவதில்லை.
கலவைகள்
அரிய-பூமி கூறுகள் பல்லாயிரக்கணக்கான சேர்மங்களை வலதுபுறத்தில் உள்ள அனைத்து உறுப்புகளுடன் உருவாக்குகின்றன - மற்றும் அவ்வப்போது அட்டவணையில் குழு 7 உலோகங்கள் (மாங்கனீசு, டெக்னீடியம் மற்றும் ரீனியம்), மற்றும் பெரிலியம் மற்றும் மெக்னீசியம் ஆகியவை அடங்கும். குழு 2 இல் இடது புறம். முக்கியமான கலவை தொடர் மற்றும் தனித்துவமான பண்புகள் அல்லது அசாதாரண நடத்தைகள் கொண்ட சில தனிப்பட்ட கலவைகள் கீழே விவரிக்கப்பட்டுள்ளன.
ஆக்சைடுகள்
இன்றுவரை ஆய்வு செய்யப்பட்ட கனிம அரிய-பூமி சேர்மங்களின் மிகப்பெரிய குடும்பம் ஆக்சைடுகள் ஆகும். மிகவும் பொதுவான ஸ்டோச்சியோமெட்ரி ஆர் 2 ஓ 3 கலவை ஆகும், ஆனால், ஒரு சில லாந்தனைடு கூறுகள் 3+ ஐத் தவிர மற்ற வேலன்ஸ் நிலைகளைக் கொண்டிருப்பதால், பிற ஸ்டோச்சியோமெட்ரிகள் உள்ளன-உதாரணமாக, சீரியம் ஆக்சைடு (சிஓஓ 2), பிரசோடைமியம் ஆக்சைடு (பிஆர் 6 ஓ 11), டெர்பியம் ஆக்சைடு (Tb 4 O 7), யூரோபியம் ஆக்சைடு (EuO), மற்றும் Eu 3 O 4. பெரும்பாலான விவாதங்கள் பைனரி ஆக்சைடுகளை மையமாகக் கொண்டிருக்கும், ஆனால் மும்மை மற்றும் பிற உயர்-வரிசை ஆக்சைடுகளும் சுருக்கமாக மதிப்பாய்வு செய்யப்படும்.