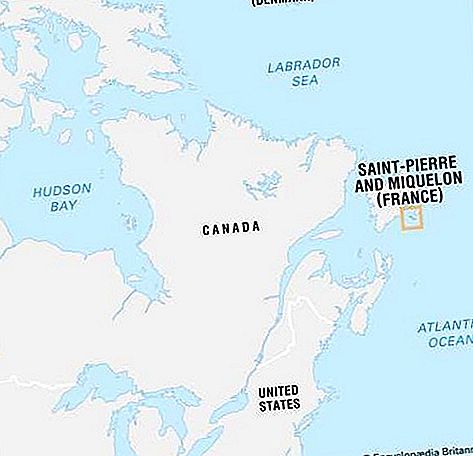
வண்ண மையம், ஒரு குறிப்பிட்ட நிறத்தின் அல்லது அகச்சிவப்பு அல்லது புற ஊதா கதிர்வீச்சின் புலப்படும் ஒளியை உறிஞ்சும் திடப்பொருளுக்குள் அணுக்களின் வழக்கமான இடைவெளியில் உள்ள குறைபாடு, இதனால் திடத்திற்கு ஒரு சிறப்பியல்பு நிறத்தை அளிக்கிறது. ஒவ்வொரு வண்ண மையத்திலும் அது பொதுவாக திடப்பொருளில் ஆக்கிரமிக்கும் இடத்திலிருந்து ஒரு அணு இல்லாதது மற்றும் அத்தகைய வெற்று இடம் அல்லது காலியிடத்துடன் ஒரு எலக்ட்ரானின் உறவை உள்ளடக்கியது. தூய்மையற்ற அணுக்கள் அல்லது ஒளியை உறிஞ்சும் பிற கட்டமைப்புகள் இருந்தால் வண்ண மையங்கள் இல்லாத திடப்பொருட்களுக்கு இன்னும் வண்ணம் இருக்கலாம்.
நிறம்: வண்ண மையங்கள்
ஒரு வண்ண மையத்தில் பெரும்பாலும் சோடியம் குளோரைடு போன்ற ஒரு அணுவைக் காணாத ஒரு திடப்பொருள் அடங்கும், இது ஒரு முப்பரிமாணத்தைக் கொண்ட அயனி படிகமாகும்
பல வகையான வண்ண மையங்கள் உள்ளன. எஃப்-சென்டர் (ஜெர்மன் ஃபார்பே, “நிறம்”) என அழைக்கப்படும் மிகச் சிறந்த புரிந்துகொள்ளப்பட்ட ஒன்று, அயனி திடப்பொருளில் ஒரு குறிப்பிட்ட புள்ளியிலிருந்து எதிர்மறையாக சார்ஜ் செய்யப்பட்ட அயனி இல்லாததன் விளைவாகும். நேர்மறையாக சார்ஜ் செய்யப்பட்ட துகள் போல செயல்படும் இந்த காலியிடம் ஒரு எலக்ட்ரானை ஈர்க்கிறது மற்றும் சிக்க வைக்கிறது, அவற்றின் கலவையானது ஒரு எஃப்-மையமாக அமைகிறது. அவ்வாறு சிக்கியுள்ள எலக்ட்ரான் ஒளியின் சில வண்ணங்களை மட்டுமே உறிஞ்சும். சோடியம் குளோரைடில் உள்ள எஃப்-மையங்கள் நீல ஒளியை மட்டுமே உறிஞ்சி, திடத்திற்கு மஞ்சள்-ஆரஞ்சு நிறத்தைக் கொடுக்கும். சோடியம் குளோரைடு பொதுவாக நிறமற்றது, இருப்பினும், அதன் எலக்ட்ரான்கள் திடப்பொருளிலிருந்து எதிர்மறை குளோரைடு அயனிகளை அகற்றுவதன் மூலம் உருவாகும் காலியிடங்களுக்கு செல்ல இலவசமல்ல. திடத்தைத் தாக்கும் எக்ஸ்-கதிர்கள், எடுத்துக்காட்டாக, எலக்ட்ரான்களை விடுவிப்பதன் மூலம் வண்ண மையங்களை உருவாக்கக்கூடும்.